| Главная | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Введение в природоведческую микробиологию2. ЭНЕРГЕТИЧЕСКИЕ МЕХАНИЗМЫ Реакции энергетического обмена представляют важнейшую функцию микроорганизмов, связанную с их преимущественно химическим взаимодействием со средой. Это взаимодействие полностью определяется термодинамическими закономерностями. Бактерии удивительно полно используют возможности получения энергии, но в этом отношении действует ряд ограничений, обусловленных способами ее превращения. Источниками энергии для организмов могут служить свет и восстановленные химические соединения. Способность использовать энергию света свойственна фотосинтезирующим микроорганизмам, представляющим несколько филогенетически и функционально различных групп. Наибольшее распространение получил оксигенный фотосинтез, осуществляемый цианобактериями и всеми фототрофными эукариотами. Для природоведческой микробиологии его значение связано прежде всего с первичной продукцией, представляющей исходный этап большинства трофических цепей, и с образованием молекулярного кислорода, обеспечивающего существование аэробов. Способность использовать химическую энергию присуща всем без исключения организмам. Особенно многообразны возможности прокариот. Это относится как к природе окисляемых субстратов, которыми могут быть неорганические (например, Н2, S2-, S0, S2О3-2, NH3, Fe2+, CO) или многочисленные органические соединения, так и окислителей (О2 Fe3+, NO3-, SO42, S0, CO2, органические вещества). Организмы используют в первую очередь субстраты, дающие наибольший выигрыш энергии. 2.1. ТЕРМОДИНАМИКА ХЕМОТРОФНЫХ МИКРООРГАНИЗМОВ. (НЕКОТОРЫЕ ТЕРМОДИНАМИЧЕСКИЕ СООБРАЖЕНИЯ) Возможность использовать энергию химической реакции для роста организмов определяется изменением свободной энергии, AG (т.е. той энергией, которая при постоянном давлении и температуре может быть превращена в работу). Понятие свободной 27 энергии является одним из центральных понятий термодинамики, оно достаточно подробно обсуждается в руководствах по физической химии. Применительно к биологическим системам можно рекомендовать соответствующие главы "Биохимии" А. Ленинджера (1970). Изменение свободной энергии в реакции A+B=C+D может быть вычислено через константу равновесия реакции как:
ΔG = ΔG° + 2,ЗОЗRT lg К = ΔG + 2,303 lg 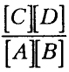 , ,
где R - газовая постоянная; Т - абсолютная температура в градусах Кальвина; К - константа равновесия реакции; [А], [В], [С], [D] - концентрации субстратов (А, В) и продуктов (С, D) реакции; ΔG° - стандартное изменение свободной энергии, рассчитанное для стандартных условий реакции: давлении 1 атм и 1 М концентрации всех реагирующих веществ; ΔG° = 2,303RT lg К, и эта величина является постоянной характеристикой реакции. Для обозначения стандартной свободной энергии при рН 7, что соответствует физиологическим условиям, используют символ ΔG°. Важнейшим следствием приведенного уравнения является зависимость роста микроорганизмов от удаления продуктов реакции, что достигается их взаимодействием с микроорганизмами, потребляющими эти продукты. Другим вариантом служит удаление продуктов в виде газов или образование нерастворимых минералов. Эти закономерности применимы не только к одной реакции, но и к цепочке реакций, осуществляемых сообществом. Изменение стандартной свободной энергии может быть также определено как разность между свободной энергией исходных веществ и свободной энергией продуктов реакции при стандартных условиях. Значения свободной энергии ряда соединений, часто используемых в метаболизме микроорганизмов, приведены В табл. 1. 28 Таблица 1 Свободные энергии образования важнейших соединений1
1 кал = 4,184 Дж
29 Связь стандартной свободной энергии реакции с окислительно-восстановительным потенциалом выражается уравнением:
ΔG°' = nF ΔE0',
где п - число перенесенных протонов; F - число Фарадея; ΔE0' - разность стандартных окислительно-восстановительных потенциалов (E0') акцептора и донора электронов (табл. 2). В условиях контакта с атмосферой веществом, задающим окислительно-восстановительный потенциал, в первую очередь, является О2. Таблица 2 Окислительно-восстановительные потенциалы
30 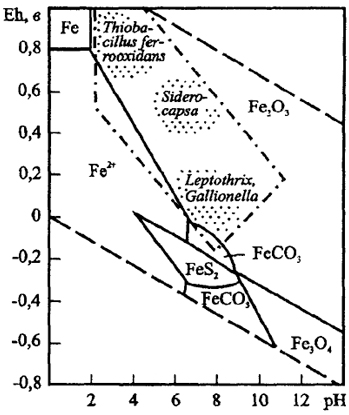 Рис.3. Поля устойчивости соединений железа в координатах Eh-pH Показаны области развития основных групп железобактерий. Пунктир - поле устойчивости воды Для природоведческой микробиологии важнейшим показателем служит окислительно-восстановительное состояние среды обитания микроорганизмов. Для реакций неорганических веществ были рассчитаны поля устойчивости соединений и минералов в координатах окислительно-восстановительного потенциала Eh и рН (диаграммы Пурбэ). Eh характеризует восстановленность среды, а рН отражает концентрацию протонов. В качестве примера на рис. 3 приведена диаграмма устойчивости соединений железа. Микроорганизмы развиваются в поле устойчивости продукта реакции и неустойчивости (метастабилъности) субстрата. Поэтому геохимические поля устойчивости минералов и области развития микроорганизмов и их сообществ коррелируют между собой, что принципиально важно для геохимии. 31 1
Выборка из Thauer R., Jungerman К., Decker К. // Bacteriol. Rev., 1977. Vol. 41. P. 100-180.
1
no Thauer R., Jungcrman K., Decker K. 1977.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||